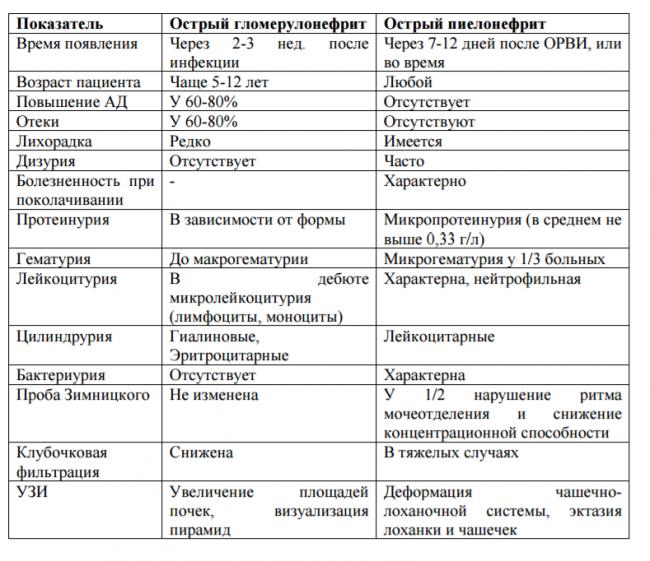
Постстрептококковый гломерулонефрит — это патологическое состояние организма, связанное с образованием иммунных комплексов (ассоциация антиген-антитело) в клубочково-фильтрационной системе почек, вследствие воздействия на него бета-гемолитического стрептококка или продуктов его жизнедеятельности.
Причины развития
 Перед тем как разобраться с основным этиологическим фактором возникновения болезни, необходимо понимать, что в большинстве случаев постстрептококковый гломерулонефрит возникает у детей или в юношеском возрасте, причем мальчики болеют в 1,5–2 раза чаще девочек. Реже постстрептококковая форма развивается при беременности.
Перед тем как разобраться с основным этиологическим фактором возникновения болезни, необходимо понимать, что в большинстве случаев постстрептококковый гломерулонефрит возникает у детей или в юношеском возрасте, причем мальчики болеют в 1,5–2 раза чаще девочек. Реже постстрептококковая форма развивается при беременности.
Острый постстрептококковый гломерулонефрит у детей происходит после перенесенной соответствующей стрептококковой инфекции, а именно:
- острый и хронический тонзиллит;
- скарлатина, гайморит;
- ринит;
- другие инфекционные заболевания верхних дыхательных путей.
Довольно редко этот синдромный комплекс может возникнуть после остеомиелита, пиодермии и гнойного отита.
Острый гломерулонефрит постстрептококковой формы возникает вследствие контакта организма человека с бета-гемолитическим стрептококком группы А или штаммом №12, что подтверждается иммунологическими методами исследования.
Развитие постстрептококковой формы
После контакта нашего организма со штаммом стрептококка, иммунной системой начинают рефлекторно синтезироваться специфические антитела, которые впоследствии вступают в контакт с антигенами микроба и образуют систему комплемента, вызывающую характерную острую постстрептококковую форму гломерулонефрита.
Интересно знать, что антигены стрептококка взаимодействуют с такими же антигенами клубочков (гломерул) почек и ранее синтезированные нашим организмом антитела вступают в реакцию с собственными антигенами, то есть появляется так называемая ауто агрессия иммунной системы против самой себя. Благодаря такому эффекту возникает тотальное повреждение всех микроскопических структур почки, включая гломерулы.
Когда организм начинает «убивать» собственные ткани почки, в последствие чего они отмирают, то обратно включается система синтеза антител, но только еще и с участием почек. В результате получается так называемый «порочный круг».
В дальнейшем, даже после стихания аутоиммунного процесса, он может включаться обратно, как реакция на воздействие агрессивных факторов внешней среды. Как пример, переохлаждение, интоксикация чем-либо или развитие какого-либо инфекционных заболеваний. Указанные выше комплементы быстро фиксируются к стенкам сосудов клубочков, разрушая их при этом. И снова возникает процесс, направленный на борьбу самим с собой.
Клиническая картина
В классическом виде, постстрептококковый гломерулонефрит начинает развиваться спустя 10–14 дней после перенесенной инфекции. Важно знать, что клиника острого постстрептококкового гломерулонефрита может проходить двумя разными путями: циклично и ациклично. В первом случае болезнь протекает с тремя последовательными стадиями, что внешне проявляется признаками:
- Нефритический синдром (отеки тканей, гипертензия и патологические изменения со стороны сердечно-сосудистой и центральной нервной системы) и типичные почечные симптомы:
- уменьшение общего количества выделяемой мочи, кровь, белок и цилиндрический эпителий в ней;
- признаки общей интоксикации (вялость, боли в голове и пояснице, отсутствие аппетита);
- сильная жажда и несоответствие выпитой жидкости к выделенной почками.
2. Обратное развитие процесса, то есть начинается полиурия (увеличение мочи):
- снижается макрогематурия, понемногу уменьшается отечность и артериальное давление возобновляется до нормальных цифр;
- начинают исчезать симптомы интоксикации, описанные выше.
Спустя 1-2 месяца после лечения, все показатели почки полностью нормализуются и организм начинает самовосстановление. Если в указанные сроки этого не случается, то острая стадия постстрептококкового гломерулонефрита переходит в хроническую.
Если происходит ациклическое течение острой формы болезни, то процесс характеризуется мочевым синдромом (изменение состава мочи, уменьшение ее количества и прочее), в большей степени отсутствуют экстраренальные симптомы.
Возможные осложнения:
- острая почечная недостаточность;
- инфекционно-токсический шок;
- гипертонический криз и инсульт;
- острая сосудистая и сердечная недостаточность.
Методы диагностики заболевания
Диагностирование острого постстрептококкового гломерулонефрита является нетрудной задачей, которая может быть выполнена с помощью общего и биохимического анализа крови, мочи, иммунологического исследования и применения тонкоигольной пункции под контролем УЗИ для гистологического подтверждения.
Также как и при обычном гломерулонефрите, в крови присутствует лейкоцитоз и незначительная анемия, а также снижение количества протеина или полное его отсутствие, повышение уровня азота и мочевины. В моче определяются различные оксалаты, осадок и значительное количество красных кровяных телец. Выявление в крови антител к почечной ткани и иммунологические комплексы свидетельствуют также о специфичности воспалительного процесса.
Наиболее точным методом является тонкоигольная биопсия под контролем ультразвука, которая подтвердит как обычный, так и постстрептококковую форму гломерулонефрита. Помимо этого, с помощью доплеровского ультразвукового исследования можно определить степень нарушения кровотока.
Терапия
 Лечение острого постстрептококкового гломерулонефрита начинается прежде всего из выявления переносчика этого микроорганизма: родственниками или окружающими его людьми. Следующим этапом терапии будет снижение и постоянная регуляция артериального давления, что достигается путем назначения антигипертензивных препаратов различных классов (блокаторы кальциевых каналов, ингибиторы АПФ, бета-блокаторы, мочегонные). Лечение этой патологии должно идти параллельно с коррекцией водно-солевого баланса и снижения отеков тканей и органов.
Лечение острого постстрептококкового гломерулонефрита начинается прежде всего из выявления переносчика этого микроорганизма: родственниками или окружающими его людьми. Следующим этапом терапии будет снижение и постоянная регуляция артериального давления, что достигается путем назначения антигипертензивных препаратов различных классов (блокаторы кальциевых каналов, ингибиторы АПФ, бета-блокаторы, мочегонные). Лечение этой патологии должно идти параллельно с коррекцией водно-солевого баланса и снижения отеков тканей и органов.
При точном диагностировании постстрептококкового гломерулонефрита, в обязательном порядке проводится антибактериальная терапия, направленная на остановку развития инфекции в организме, путем назначения бактериостатических препаратов, но не бактерицидных. Это объясняется тем, что бактериостатики останавливают репликацию стрептококка, но не убивают его, в противном случае продукты распада этих микробов начнут пагубно воздействовать на организм, последний будет отвечать на них бурной аллергической реакцией.
Лечение острого постстрептококкового гломерулонефрита также включает в себя и подавление иммунной системы человека путем введения больших доз стероидных гормонов (преднизолон, дексаметазон, адреналин, гидрокортизон). Это делается для уменьшения циркуляции иммунных комплексов в крови, что приводит к началу процессов регенерации.
Не стоит забывать и о диетическом лечении. Диета при остром постстрептококковым гломерулонефрите включает в себя стол №7, характеризующийся малым количеством животного белка и мяса, а также большим содержанием растительной пищи. Соль при этом столе показана в минимальных дозах.
Прогноз и профилактика
Если больной не получает своевременного лечения, то острая форма гломерулонефрита переходит в хроническую, что неизбежно приведет к развитию почечной недостаточности и смерти.
В качестве профилактики рекомендуется:
- избегать переохлаждений;
- своевременная санация верхних дыхательных путей при воспалении последних;
- адекватное лечение тонзиллитов, отитов и фарингитов;
- укрепление общего состояния человека путем закаливания.
Лечение и профилактика острого постстрептококкового гломерулонефрита у детей требует пристального внимания как самого больного, так и специалиста. При этом для предотвращения угрожающих жизни осложнений, пациенты с постстрептококковой формой должны постоянно находится под присмотром лечащего врача.
<index>
Обычно мертвые бактерии и антитела выводятся из организма без проблем. Однако в случае с постстрептококковым гломерулонефритом они попадают в ловушку почечных клубочков, что приводит к замедленной фильтрации почек, развитию локального внутрисосудистого свертывания крови и микротромбозу.
Вероятность развития постстрептококковой инфекции у женщин при вынашивании плода незначительна.
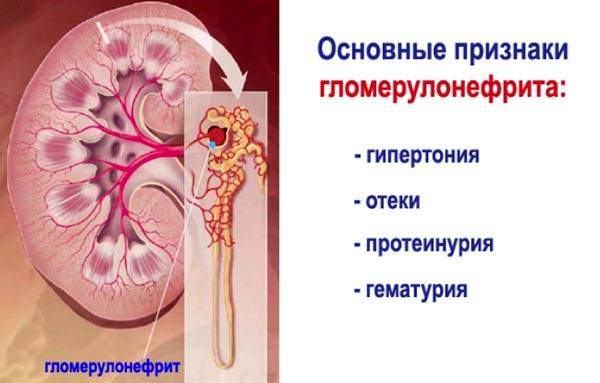 ОПСГ — проявления заболевания
ОПСГ — проявления заболевания
Острый постстрептококковый гломерулонефрит у детей напрямую связывают с:
- тонзиллитом в острой или хронической форме;
- воспалением гайморовых пазух;
- скарлатиной;
- инфекционными воспалениями дыхательных путей.
В редких случаях данный вид заболевания может произойти на фоне гнойно-некротических процессов в костном мозге, гнойных поражений кожи и отита с гнойной этиологией.
Острая форма
Данная болезнь характеризуется воспалением почечных клубочков с обеих сторон и развивается на фоне стрептококковой инфекции. Она характерна для мальчиков и молодых людей в возрасте от 14 до 35 лет. Нередко регистрируется острый постстрептококковый гломерулонефрит и в детском возрасте, в 6-10 лет. Его напрямую связывают с возможным переохлаждением. Заболевание чаще встречается в регионах с повышенной влажностью.
Развитие патологии происходит в 35 случаях на 1000 населения. В период весенне-зимних холодов воспалительный процесс в органах мочевыделения провоцируется острыми респираторными вирусными инфекциями, а летом и осенью – появляются гнойничковые воспаления на поверхности кожи.
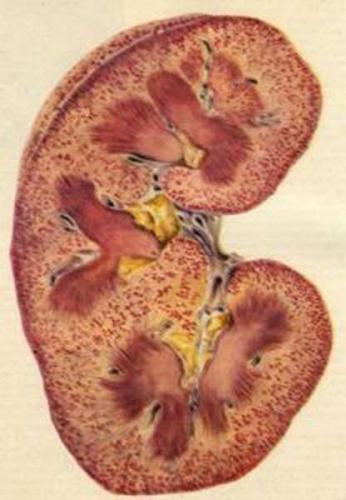
Состояние тканей почки при ОПСГ — под микроскопом
Формы заболевания
Острый постстрептококковый гломерулонефрит – не очень распространенное заболевание, но иногда носит эпидемический характер.
- Пролиферативный диффузный гломерулонефрит характерен для детей от 3 до 7 лет.
- Субклинический гломерулонефрит чаще всего поражает более старшее население мужского пола.
Причины возникновения
Самой частой причиной появления постстрептококкового острого гломерулонефрита является наличие инфекции, вызванной стрептококком. После попадания в организм человека нефритогенные виды стрептококков обуславливают возникновение очагов воспалительного характера.
Поражаются почки, нарушаются их функции. Патологический процесс длится на протяжении нескольких недель после таких перенесенных инфекционных заболеваний, как ангина, скарлатина или гнойничковые поражения кожи.
Происхождение
Описанный выше вид постстрептококкового гломерулонефрита часто возникает по причине попадания в организм стрептококков, относящихся к группе А. В дальнейшем организмом начинают активно вырабатываться антитела, вступающие во взаимосвязь с антигенами. Такие виды патологических процессов ведут к появлению специфических иммунных комплексов, воздействующих на паренхиматозные ткани почек, приводя к дальнейшему их повреждению и нарушению структуры почечных единиц – нефронов.
Схема развития ОПСГ из ангины и импетиго
Изначально инфекция развивается в виде иммунокомплексной патологии, но потом начинает принимать форму аутоантительной болезни. На этом этапе начинает развиваться аллергия. Больным необходимо помнить, что этот вид инфекционного заболевания имеет свойство регрессировать. Поэтому необходимо постоянное наблюдение у специалиста и контроль за протеканием инфекционных процессов в организме. Кроме того, нужно организовать правильную профилактиу.
Симптоматика
На протяжении 7-14 дней у больного не будет возникать никаких ярко выраженных симптомов. А потом начнут проявляться первые ренальные или же экстраренальные симптомы. К ним относят:
- изменения артериального давления;
- возникновение отеков на теле;
- нарушение в сердечно-сосудистой системе;
- появление крови в выделяемой моче;
- головные боли;
- боль в области поясничного отдела;
- уменьшение количества выделяемой мочи;
- появление белка в моче.
В начальном стадии заболевания нужно обязательно посетить специалиста и провести необходимые диагностические мероприятия, а также соответствующую терапию.
Методы диагностики
После посещения специалиста, который должен собрать анамнез и сделать визуальный осмотр, назначаются различные виды лабораторных исследований. Методы диагностики включают в себя:
- общий и биохимический анализ крови;
- общий анализ мочи;
- ультразвуковое исследование почек;
- рентгенографию;
- магнитно-резонансную томографию структуры почек;
- измерение скорости мочеиспускания.
Анализ мочи — диагностика ОПСГ
Если количество отделяемой мочи уменьшенное, в результатах лабораторных исследований урины может обнаружиться повышенное количество креатинина и мочевины. Это прямо указывает на то, что развивается почечная недостаточность. Применяя метод ультразвукового исследования, обнаруживают нарушения дифференциального типа, а также увеличение почек, причиной которого служит нарушение оттока урины.
В некоторых случаях может быть собран врачебный консилиум в составе стоматологов, офтальмологов и отоларингологов. Это необходимо для того, чтобы выявить возможные сопутствующие заболевания, такие как наличие зубного кариеса, сосудистой ангиопатии сетчатки и прочих.
Лечение и его виды
Назначают лечение постстрептококкового гломерулонефрита после того, как выявили возбудителя и определили, от кого из родственников больной мог инфицироваться. Наблюдают за изменениями артериального давления, назначая антигипертензивные препараты.
Проводится строгая коррекция водно-солевого баланса для снижения отечностей в тканях и внутренних органах.
Постстрептококковый гломерулонефрит связан с бактериальной инфекцией, поэтому назначают антибиотикотерапию. Чаще применяют препараты пенициллиновой группы, такие как феноксиметилпенициллин и эритромицин. Применение этих медикаментозных средств показано при тонзиллите или фарингите, а также гнойничковых инфекциях кожи.
Практикуется применение стероидных гормональных препаратов, таких как:
- преднизолон;
- дексаметазон;
- адреналин;
- гидрокортизон.
Эти меры необходимы для того, чтобы подавить реакцию иммунной системы организма.
Схема лечения ОПСГ антибиотиками
Важным этапом лечения острого заболевания является соблюдение специальной диеты. Она основана на снижении количества потребляемого белка животного происхождения и введении в рацион большого количества растительной пищи. Исключается потребление соли. Также желательно отказаться от жареной, жирной и копченой пищи.
Прогноз и меры профилактики
При несвоевременном лечении острая форма болезни перетекает в хроническую. Это влечет за собой дальнейшее развитие дисфункции в почках, а также появление почечной недостаточности. В отдельных случаях может привести к летальному исходу.
Отмечено, что детский организм намного успешнее борется с недугом.
После проведенного лечения необходимо посещать врача один раз в полгода.
Острый гломерулонефрит возникает при различных заболеваниях инфекционного характера, в том числе вследствие эндокардита, вызванного Streptococcus viridans, инфицирования Staphylococcus epidermalis в результате проведения шунтирования при гидроцефалии, а также сифилиса, гепатита В и С. Кроме того, при возникновении гломерулонефрита играют важную роль различные виды паразитарных инвазий, таких как возбудители малярии, лейшманиоза, филяриоза, эхинококкоза. В таком случае процесс будет хроническим.
Летальный исход может быть в 3% случаев от всех заболевших.
У маленьких детей в 95% наблюдается положительная динамика при правильном и своевременном лечении. У пациентов после 35 лет данный вид заболевания имеет более сложную картину, и выздоровление наступает гораздо реже.
Для профилактики заболевания нужно:
- избегать переохлаждения;
- своевременно лечить воспаления верхних дыхательных путей;
- лечить тонзиллиты, отиты и фарингиты;
- укреплять иммунитет.
</index>
Острый постстрептококковый гломерулонефрит у детей
Большинство случаев спорадические, эпидемические вспышки возникают редко. Зимой и весной возникновение постстрептококкового гломерулонефрита ассоциируется с ОРВИ, летом и осенью — с пиодермией. В последние десятилетия в развитых странах отмечается снижение частоты гломерулонефритов до 10-15% всех гломерулонефритов, что связано с улучшением социально-экономических условий. В развивающихся странах постстрептококковый гломерулонефрит — причина 40-70% всех гломерулонефритов. Пик заболеваемости приходится на дошкольный и младший школьный возраст (5-9 лет), менее 5% детей переносят гломерулонефрит до 2-летнего возраста. Постстрептококковый гломерулонефрит в 2 раза чаще бывает у мальчиков. В последние годы в России увеличилась заболеваемость острым постстрептококковым гломерулонефритом, что связано с увеличением частоты стрептококковой инфекции у детей из-за появления устойчивых штаммов к основным антибактериальным препаратам, используемым в клинической практике.
Этиологический фактор удаётся установить в 80-90% случаев острого гломерулонефрита и лишь в 5-10% — хронического.
Основные этиологические факторы острого гломерулонефрита
- Инфекционные.
- Бактерии: бета-гемолитический стрептококк группы А, энтерококки, пневмококки, стафилококки, коринебактерии, клебсиеллы, сальмонеллы, микоплазмы, иерсении, менингококки.
- Вирусы: гепатита В, кори, Эпштейна-Барр, Коксаки, краснухи, ветряной оспы, цитомегаловирус, реже — вирус простого герпеса.
- Паразиты: плазмодии малярии, токсоплазмы, шистосомы.
- Грибы: кандида.
- Неинфекционные.
- Чужеродные белки.
- Сыворотки.
Наиболее частая причина развития острого гломерулонефрита у детей — перенесённая стрептококковая инфекция, поэтому во всех руководствах выделяют острый постстрептококковый ГН. Чаще всего за 1-3 нед до острого гломерулонефрита дети переносят ангину, фарингит, кожные инфекции, реже — скарлатину. Эти заболевания вызывает бета-гемолитический стрептококк группы А, чаще всего М-типа штаммов 1, 3, 4, 6, 12, 25, 49 после инфекций верхних дыхательных путей, а также М-типа штаммов 2, 49, 55 после кожных инфекций. Эти типы называют нефритогенными, из них наиболее часто встречаются штаммы 12 и 49.
Другие бактериальные антигены вызывают заболевание реже.
Разрешающими факторами могут быть: охлаждение, чрезмерная инсоляция, физическая травма.
Пик заболевания острым гломерулонефритом у детей приходится на осенне-зимний период, при низких температурах и повышенной влажности.
Предрасполагающими факторами развития ОПСГН являются:
отягощенная наследственность в отношении инфекционно-аллергических заболеваний; повышенная семейная восприимчивость к стрептококковой инфекции; наличие у ребенка хронических очагов инфекции; гиповитаминозы, гельминтозы; частые ОРИ; охлаждения.
Патогенез
Иммунокомплексный механизм , при этом растворимые иммунные комплексы «антиген-антитело» откладываются в клубочках.
Иммунные комплексы привлекают в очаг их отложения клетки воспаления (нейтрофилы, моноциты, тромбоциты), которые вырабатывают провоспалительные цитокины (ИЛ-1, ФНО, ТФР-а). Цитокины активируют накопление вазоактивных субстанций, что приводит к повреждению, возникновению трещин и повышению проницаемости базальных мембран. Почка отвечает на повреждение пролиферацией мезангиальных и эндотелиальных клеток. Развивается воспалительный инфильтрат. Повреждение эндотелия капилляров приводит к локальной активации системы коагуляции и пристеночному тромбообразованию, сужению просвета сосудов. В результате воспаления возникают гематурия, протеинурия и нарушение функции почек. Развивается картина острого пролиферативного ГН, чаще с клинической картиной ОНС.
2 синдрома, нефритический характеризует постстрептококковый ГН
— Нефротический
- отеки (распространенные, вплоть до анасарки)
- протеинурию массивную, выше 3,5 г/с, у детей выше 50 мг/кг/с
- гипопротеинемию (менее 40 г/л), гипоальбуминемию (менее 30 г/л), гипер ά2глобулинемию
- гиперхолестеринемию (гиперлипидемию)
— Нефритический
- Гематурией (макро, микрогематурией)
- Протеинурией (умеренной)
- Отеками (чаще умеренными)
- Артериальной гипертензией
- Быстрым снижением скорости клубочковой фильтрации и азотемией
Начало заболевания может быть бурным, острым, с классической триадой симптомов: отёки, артериальная гипертензия, макрогематурия. Дети жалуются на недомогание, головную боль, тошноту, рвоту, изменение цвета мочи, уменьшение её количества. Степень выраженности этих симптомов бывает разная.
Реже происходит постепенное развитие заболевания со скудными клиническими и лабораторными изменениями.
При осмотре всегда обнаруживают отёки век, голени, бледность кожных покровов в результате спазма сосудов. Спазм сосудов выражен и на сетчатке глазного дна. Больные могут жаловаться на головную боль и боль в пояснице, что объясняется растяжением капсулы почек в связи с их отёком.
Главными следствиями развившегося воспалительного процесса в почках являются снижение клубочковой фильтрации, и формирование основных синдромов ОПСГН – мочевого, отечного и гипертензионного.
Отёки
Отёки — одно из основных проявлений ОНС — возникают у 60-80% больных. Степень выраженности может варьироваться в широких пределах: от отёков век по утрам до выраженной отёчности лица, голеней, передней брюшной стенки. Очень редко, но могут развиваться полостные отёки: гидроторакс, гидроперикард, асцит. За период нарастания отёков больные могут прибавить в весе 2-5 кг. Появление отёков происходит постепенно. Они плотные, малоподвижные.
Механизм формирования отёков:
- увеличение объёма циркулирующей крови в результате снижения клубочковой фильтрации — гиперволемия;
- задержка натрия и воды (гиперальдостеронизм, повышение секреции АДГ);
- повышенная сосудистая проницаемость в результате гиалурони- дазной активности стрептококка, выброса гистамина и активации калликреин-кининовой системы.
Образование периферических отёков можно рассматривать как компенсаторный механизм, так как часть жидкости из сосудисто-го русла перемещается в ткани, уменьшая гиперволемию, и это препятствует развитию осложнений. С депонированием жидкости может быть также связано увеличение печени и селезёнки. Отёки обычно легко купировать назначением бессолевой диеты и диуре-тических препаратов. Длительность отёков составляет 5-14 дней.
Артериальная гипертензия
Артериальная гипертензия — один из грозных симптомов острого гломерулонефрита (ОГН) — возникает у 60-70% больных. Больные жалуются на головную боль, тошноту, рвоту. Развитие артериальной гипертензии происходит быстро. С ней чаще всего связаны осложнения: эклампсия и острая сердечная недостаточность. Артериальная гипертензия носит систоло-диастолический характер, но с большим подъёмом систолического давления. Механизм артериальной гипертензии при ОНС:
- гиперволемия, т.е. увеличение объёма циркулирующей крови (ОЦК), происходит в связи с падением клубочковой фильтрации, задержкой воды и натрия;
- гораздо меньшую роль играет активация ренин-ангиотензин-альдостероновой системы.
В силу того, что основным механизмом развития артериальной гипертензии служит гиперволемия, она легко поддаётся лечению (бессолевая диета, диуретики), реже возникает необходимость в назначении антигипертензивных препаратов. Нельзя вводить препараты, увеличивающие ОЦК. Длительность гипертензионного синдрома — 7-14 дней.
Мочевой синдром
Олигурия — уменьшение нормального диуреза на 20-50% нормы. Возникает олигурия в связи с падением клубочковой фильтрации и повышенной реабсорбцией воды и натрия, развитием «антидиуреза» и повышением секреции АДГ. Относительная плотность мочи высокая. Олигурия возникает в первые дни заболевания и длится 3-7 дней.
Гематурия — одно из главных проявлений мочевого синдрома — возникает у 100% больных. Макрогематурию обнаруживают в начале заболевания у 60-80% больных, её выраженность постепенно уменьшается к 3-4-й неделе. У основной массы больных гематурия полностью прекращается к 8-10-й неделе, однако у некоторых микрогематурия остаётся в течение 6-12 мес.
Гематурия связана с повышенной проницаемостью БМ, её разрывами. В моче появляются дисморфичные эритроциты (изменённые, неправильной формы), что обусловлено их гломерулярным происхождением. Могут встречаться также эритроцитарные цилиндры.
Протеинурия — один из ведущих признаков поражения почек, во всех случаях необходимо установить суточную потерю белка. В норме она составляет 100-200 мг/сут. При ОНС суточная протеинурия колеблется в пределах от 1 до 2,5 г/сут. Белок, теряемый с мочой, плазменного происхождения и содержит мелкие и крупные белки, т.е. протеинурия неселективная. Ведущим механизмом протеинурии служат структурные изменения базальной мембраны (увеличение размеров пор, трещины) и функциональные изменения (потеря отрицательного заряда). Протеинурия постепенно уменьшается к 2-3-й неделе заболевания. Длительная протеинурия до 1,5-2 г/сут — плохой прогностический признак.
Лейкоцитурия при ОНС может возникать в первую неделю заболевания и имеет абактериальную природу. Она объясняется активным иммунным воспалением с привлечением на 1-2-й неделе в очаг воспаления нейтрофилов, лимфоцитов, моноцитов.
Цилиндрурия может присутствовать (30-60%) в начальном периоде. По своей структуре цилиндры — это тубулярный белок (уропротеин Тамма-Хорсфалла) с включением форменных элементов, эпителиальных клеток, детрита. При ОГН могут появлятся эритроцитарные, зернистые цилиндры.
Выделяют два варианта течения ОПСГН – циклическое (типичное) и ациклическое (моносимптомное).
В типичных случаях анамнез позволяет выявить предшествующее стрептококковое поражение зева, кожи и т. д.
Объективно: ребенок бледен (за счет ангиоспазма), отеки, локализованные на лице и голенях.
Отеки бывают «скрытыми» (выявляются положительной пробой Макклюра- Олдрича).
Со стороны сердечно-сосудистой системы обнаруживается тахикардия, реже брадикардия, приглушенность тонов, расширение границ относительной сердечной тупости, ослабление I тона на верхушке, усиление 2-го типа на аорте и легочной артерии, расширение границ сердца (за счет повышения артериального давления). В некоторых случаях развивается недостаточность кровообращения.
Моча цвета «мясных помоев» (макрогематурия).
Олигурия диагностируется у половины детей, через 3-7 дней отмечается восстановление диуреза.
В периоде обратного развития симптомов появляется полиурия, купируются отеки, исчезает артериальная гипертензия, экстраренальные проявления заболевания (головные боли, нарушение самочувствия и др.).
В последнюю очередь исчезает гематурия.
Полное восстановление морфологических изменений в почках происходит через 1-2 года.
Ациклический вариант ОПСГН протекает, часто с изолированным мочевым синдромом. Заболевание характеризуется постепенным началом при отсутствии субъективных симптомов и экстраренальных проявлений. Через несколько лет может сформироваться хронический гломерулонефрит в различных формах. Основными клиническими вариантами ОПСГН являются: нефротический и нефритический синдромы
Диагноз ОПСГН основывается на выявлении перенесенной стрептококковой инфекции и латентного периода после нее.
Характерная триада симптомов (гематурия, умеренные отеки, повышение артериального давления) дает основание заподозрить ОГН.
Лабораторные исследования
Общий анализ мочи. При ОПСГН чаще всего выявляют гематурию, а в начале заболевания и лейкоцитурию. Лейкоцитурия — маркер иммунно-воспалительного процесса в почках. Для ОГН характерной находкой является цилиндрурия (гиалиновые, зернистые, эритроцитарные). У многих больных обнаруживается протеинурия до 1-2 г/л/сутки.
В анализе крови: увеличение СОЭ, нейтрофилез; при наличии инфекционного очага – лейкоцитоз, умеренная анемия.
Биохимические исследования. Наблюдается диспротеинемия за счет умеренной гипоальбуминемии, гипер-α2 и γ-глобулинемии.
При развитии выраженной олигурии у части больных в крови повышается уровень мочевины и креатинина, что рассматривается как нарушение функции почек острого периода. Возможно развитие ОПН.
При серологическом исследовании у 60-90% больных повышаются титры антистрептолизина О. Анти-М-протеиновые антитела появляются через 4-6 недель после перенесенной стрептококковой инфекции и сохраняются длительно.
У 90% больных в крови повышаются ЦИК.
В течение первых двух недель заболевания снижается уровень С2, С3, С4, фракций комплемента, который продолжается 4-6 недель. Нарушения в системе свертывания характеризуются: увеличением протромбинового индекса, снижением уровня антитромбина III, угнетением фибринолитической активности, появлением в крови продуктов деградации фибриногена. При УЗИ можно выявить незначительное увеличение почек в размерах, повышение их эхогенности.
Диагностические трудности возникают при латентном, ациклическом варианте течения заболевания.
Биопсия почки — прижизненное морфологическое исследование почечной ткани с помощью чрезкожной пункции (закрытая биопсия) или оперативным методом (открытая, полуоткрытая биопсия).
Показания для биопсии при ОПСГН: атипичные проявления гломерулонефрита, возраст до 3 лет, анурия, высокая азотемия, несоразмерная клинической картине; нарушения роста, гломерулонефрит в семье, длительное сохранение симптомов (задержка ремиссии), признаки системного заболевания, длительно сохраняющиеся гематурия и протеинурия.
Дифференциальный диагноз ОПСГН проводится с: хроническим гломерулонефритом, наследственным нефритом, геморрагическим васкулитом, транзиторным мочевым синдромом на фоне острого инфекционного заболевания, острым пиелонефритом, ревматизмом, системной красной волчанкой, ревматоидным артритом, инфекционным эндокардитом, интерстициальным нефритом, быстро прогрессирующим гломерулонефритом, IgA нефропатией (болезнь Берже), гемолитико- уремическим синдромом.
Лечение.
Задачи лечения: эрадикация стрептококковой инфекции, купирование ренальных и экстраренальных проявлений ОПСГН.
Постельный режим, диета, антибактериальная терапия.
Вспомогательное лечение: средства симптоматической терапии (мочегонные, гипотензивные), витаминотерапия, антигистаминные средства, эуфиллин, дезагреганты, мембраностабилизирующие препараты, антиоксиданты.
Показания для госпитализации: лечение ОГН проводится в стационаре.
Режим. Строгий постельный режим показан при экстраренальных симптомах и макрогематурии.
Диета. Жидкость назначают из расчета диуреза предыдущего дня и потерь на перспирацию (15мл/(кг/сут) или 400 мл/(м2 /сут)) для школьников. С увеличением диуреза количество выпиваемой жидкости увеличивают. Ограничение натрия хлорида (бессолевой стол) назначают при олигурии и гипертензии. При нормализации артериального давления и увеличении диуреза разрешено подсаливание пищи (0,5-1,0 г/сут). Нормальное количество натрия хлорида (50 мг/(кг/сут)) при благоприятном варианте течения заболевания ребенок может получать с 4-5-й недели. В дебюте ОПСГН назначают стол 7а (по Певзнеру) сроком на 3-5 дней. На 3-5-7 день назначают переходный стол 7б. В рационе увеличивается количество белка и жира. В последующем больного переводят на стол 7в. Соль добавляют в готовые блюда. Ограничение белка показано при олигурии и гипертензии. На период 5-7 дней сокращают потребление белка (до 1,0-0,5 г/(кг/сут)). Целесообразно также некоторое ограничение животных белков в течение 2-3 недель. Калорийность сохраняют за счет увеличения в диете углеводов и жиров. При олигурии показано ограничение калия. Из-за опасности гиперкалиемии исключают фруктовые или овощные соки. Противопоказаны калийсберегающие препараты. После схождения отеков целесообразно обогащение диеты калием (печеный картофель, фрукты и др.).
Больным с ОПСГН необходима антибактериальная терапия предпочтительно антибиотиками пенициллинового ряда (полусинтетические пенициллины типа амоксициллина или макролиды в обычных дозах). При отсутствии очагов инфекции длительность антибактериальной терапии 7-10 дней. При наличии очагов хронической инфекции по окончании курса антибактериальной терапии (4-6 недель) можно применять бициллин-5 или бициллин-1. Длительность бициллинотерапии до 6 месяцев.
Бициллин-5 или бициллин-1 вводят 1 раз в 3 недели в дозировках: дошкольники – бициллин-5 – 750000 ЕД., бициллин-1 – 600000 ЕД.; школьники соответственно 1500000 ЕД и 1200000 ЕД. Патогенетическая терапия ОГН может быть представлена в следующем виде (табл. 1.50). Табл. 1.50.
Патогенетическая терапия ОГН
Для улучшения почечного кровотока применяют антиагреганты (курантил, персантил), которые назначают на 3-4 недели 2-3 раза в день в суточной дозе 1,5-3,0 мг/кг/сут.
Гепаринотерапия показана при: наличии признаков гиперкоагуляции; симптомов внутрипочечного (локального) внутрисосудистого свертывания крови (быстрое снижение функции почек при уменьшении содержания фибриногена и повышении содержания продуктов деградации фибрина в сыворотке крови); наличии ДВС- синдрома; выраженном отечном синдроме; выраженной гиперлипидемии.
Методы проведения гепаринотерапии: парентеральное введение (подкожно, внутримышечно) методом электрофореза (300 ЕД/кг) и методом аэрозоля (500 ЕД/кг), 100-200 ЕД/кг суточная доза в 4 инъекции. Препарат следует отменять постепенно под контролем показателей коагулограммы.
Никотиновая кислота активирует фибринолитическую систему крови, препятствует агрегации тромбоцитов, обладает сосудорасширяющим действием.
Используют электрофорез 1% раствора никотиновой кислоты на область почек. Процедуры проводят ежедневно, число процедур 7-10.
Эуфиллин увеличивает просвет сосудов почек, дает легкий мочегонный эффект, уменьшает общее периферическое сопротивление. Препарат назначают на 1-2 недели в порошках или таблетках 3 раза в день в суточной дозе: до 9 лет – 15-18 мг/(кг/сут); 9-12 лет – 10-12,5 мг/(кг/сут); старше 12 лет – 10 мг/(кг/сут); трентал, никошпан.
Назначают витамины А, группы В, Е в возрастных дозах; мембраностабилизаторы — ксидифон, димефосфон, карсил.
Мочегонные при ОПСГН используют редко. Диуретики показаны при массивных отеках, артериальной гипертензии, гипертонической энцефалопатии.
С целью увеличения диуреза назначают фуросемид (лазикс) в дозе 1,5-2,0 мг/кг внутримышечно или внутривенно 1-2 раза в сутки, затем еще 3 дня препарат вводят через рот в 1 приём.
Гипотензивные препараты показаны при уровне диастолического давления выше 95 мм рт. ст. и при гипертонической энцефалопатии.
При высокой гипертензии препаратами выбора являются каптоприл (капотен). Каптоприл назначается в суточной дозе 0,3 мг/кг/сут. Доза может быть увеличена до 2,0 мг/кг/сут в течение 3-5 дней. Возможно внутривенное введение 2,4% раствора эуфиллина на физиологическом растворе вместе с лазиксом (1-4 мг/кг).
Основа лечения артериальной гипертензии – диуретики и антагонисты кальция.
Гемодиализ при ОПСГН показан в случае отсутствия реакции на лазикс, нарастании мочевины > 20-24 ммоль/л, калия > 7 ммоль/л, фосфора > 2 ммоль/л, < натрия до 130 ммоль/л, рН крови > 7,25. Особое внимание необходимо уделить санации очагов инфекции.
Тонзилэктомия проводится через 6 месяцев после начала ремиссии ОПСГН. При ОГН с изолированным мочевым синдромом основой лечения являются антибиотики пенициллинового ряда, макролиды в сочетании с антиагрегантами. При ОГН с нефритическим синдромом основой лечения являются антибиотики пенициллинового ряда, макролиды в сочетании с антиагрегантами и прямыми антикоагулянтами.
Осложнения. При ОПСГН возможно развитие: ангиоспастической энцефалопатии, острой почечной недостаточности, острой сердечно-сосудистой недостаточности.
Исходы. Выздоровление наступает в 85-90%. Летальный исход редко (). В 10-15% случаем ОГН трансформируется в хронический гломерулонефрит. Прогноз ближайший и отдаленный при ОПСГН с нефритическим синдромом благоприятный.
Постстрептококковый гломерулонефрит представляет собой патологию клубочково-фильтрационной системы почек. Нарушения обуславливаются негативным воздействием стрептококков бета-гемолитического типа и отходами их жизнедеятельности.
 Постстрептококковый гломерулонефрит имеет несколько форм, среди них выделяют острую и скрытую. Ему подвержены как дети, так и взрослые. Первые страдают чаще. В группе риска находятся пациенты в возрасте 5-12 лет. В большинстве случаев заболевают осенью. Острый постстрептококковый гломерулонефрит более распространён у детей, проживающих на периферии, вдали от крупных населенных пунктов. Существует так называемая «семейная» форма заболевания.
Постстрептококковый гломерулонефрит имеет несколько форм, среди них выделяют острую и скрытую. Ему подвержены как дети, так и взрослые. Первые страдают чаще. В группе риска находятся пациенты в возрасте 5-12 лет. В большинстве случаев заболевают осенью. Острый постстрептококковый гломерулонефрит более распространён у детей, проживающих на периферии, вдали от крупных населенных пунктов. Существует так называемая «семейная» форма заболевания.
Причины
Необходимо отметить, что постстрептококковым гломерулонефритом чаще заболевают мальчики, чем девочки. Особое внимание специалисты уделяют беременным женщинам. В этот период времени нагрузка на печень существенно возрастает, поэтому вероятность возникновения почечных патологий увеличивается.
К факторам, провоцирующим постстрептококковый гломерулонефрит, относят:
Тонзиллит в острой и хронической фазе.</li> Ринит.</li> Гайморит.</li> Скарлатину.</li> Отит гнойного типа.</li> Остеомиелит.</li> Пиодермию.</li> Ангину.</li> Кожные недуги.</li> Фарингит.</li> Пневмонию.</li> Акушерский сепсис.</li> Поражение мягких тканей.</li>
В основе перечисленных заболеваний бактериальное заражение. Возбудители, в данном случае Streptococcus руоgenes (штаммы М-серотипы 1, 2, 4, 12, 18, 25, 49, 55, 57, 60) и коагулазаотрицательные стафилококки, вызывают эпидемические и спорадические вспышки. Вызвать гломерулонефрит могут вирусы, грибки и паразиты. Ребенок, переболевший один раз, после не заразится, так как организм выработает защитные антитела. На сегодня опасность заражения существенно снизилась из-за повсеместного использования медикаментозных препаратов из антибиотической группы.
Инфицирование затрагивает детей, чьи условия проживания не соответствуют санитарно-гигиеническим нормам. Также риск повышен при наличии в анамнезе ревматизма. Одновременно с постстрептококковым гломерулонефритом часто развиваются:
- Хронические гнойные заболевания.
- Гипокомплементемия.
- Нефротический синдром.
- Абсцесс внутренних органов.
Все начинается с проникновения возбудителя постстрептококкового гломерулонефрита в организм. Он достигает почек, которые призваны фильтровать кровь, сохранять баланс жидкостей человеческого тела и выводить вредные вещества. Поражение гломерул (почечных клубочков) провоцирует нарушения во всех системах организма.
Острый постстрептококковый гломерулонефрит – это аутоиммунный недуг, который характеризуется стремительным поражением обеих почек. Симптомы проявляются спустя 12-14 дней после избавления. Ситуация усугубляется ослабленной иммунной системой и сниженной реактивностью организма.
Иммунные комплексы, являющиеся признаком постстрептококкового гломерулонефрита, образуются в результате взаимодействия иммуноглобулинов и антигенов стрептококка. Попадая в кровеносную систему, они застревают в капиллярах, расположенных в почечных канальцах. Итогом становится их повреждение. Данный процесс сопровождается воспалением клубочков.
Фильтрация не происходит соответствующим образом, нарушается реабсорбция, организм засоряется, возникает нехватка питательных веществ. Защитные антитела при постстрептококковом гломерулонефрите неправильно реагируют на здоровые клетки почек и уничтожают их.
Симптомы и признаки
Течение постстрептококкового гломерулонефрита может быть разным. Существует несколько классификаций данной патологии. Цикличное развитие постстрептококкового гломерулонефрита подразумевает наличие трех стадий, на протяжении которых возникают следующие симптомы:
- Отеки мягких тканей.
- Проблемы с ЦНС, пищеварительной и сердечно-сосудистой системами.
- Гипертензия.
- Снижение объема выделяемой урины и обнаружение в ней цилиндрического эпителия, крови и белковых соединений.
- Боли в голове и поясничном отделе позвоночника.
- Общая слабость.
- Повышенное употребление жидкости.
- Интоксикация организма.

Клиническая картина ацикличного постстрептококкового гломерулонефрита характеризуется ренальными проявлениями и отсутствием экстраренальных признаков. К последним относят бледную окраску кожных покровов, тошноту, рвоту, ухудшение тонуса кровеносных сосудов в глазах, отечность, шумы в сердце и брадикардию. Ренальные симптомы выражаются в виде цилиндрурии, протеинурии, гематурии и олигурии. И те и другие присутствуют на первой стадии цикличного постстрептококкового гломерулонефрита.
Вторая фаза патогенеза постстрептококкового гломерулонефрита подразумевает стабилизацию общего состояния (объем урины в норме, отсутствие отеков и повышенного АД). Длительность обеих стадий не больше 1,5 месяцев. Если пациент не выздоровел по окончании второй фазы, диагностируют переход постстрептококкового гломерулонефрита в хроническую форму.
Диагностика
Диагностирование постстрептококкового гломерулонефрита происходит следующим образом:
- Сбор анамнезаНефролог опрашивает и осматривает пациента.
- Лабораторные и иммунологические исследованияОпределяют уровень антистрептококковых антител, делают биопсию почечной ткани, ОАК, ОАМ, биохимию урины и крови, гистологию, тонкоигольную пункцию, анализ мочи по Нечипоренко.
- Световая, электронная и иммунофлюоресцентная микроскопияПосредством ее выявляют диффузный пролиферативный гломерулонефрит. Чем крупнее отложения на стенках мелких кровеносных сосудов, тем серьезнее последствия.
- УЗИ.
- ЭКГ.
- Консультации других специалистов, например, офтальмолога.
Диагноз «постстрептококковый гломерулонефрит» подтверждается повышением СОЭ в моче (клинический анализ урины), холестеринемией (увеличение иммуноглобулинов), протеинурией, цилиндрурией, гематурией. В урине при постстрептококковом гломерулонефрите находят большое количество лейкоцитов.
Лечение
Схема терапевтических действий, назначаемая нефрологом при постстрептококковом гломерулонефрите, включает в себя:
- Медикаментозную терапию.
- Постельный режим.
- Корректировку рациона питания.
- Гемодиализ.
Стабилизация артериального давления происходит посредством ингибиторов АПФ, диуретиков, блокаторов кальциевых каналов (предупреждают вымывание минерала из организма), бета-блокаторов, антигипертензивных препаратов. Одновременно восстанавливают водно-солевой баланс и устраняют отечность мягких тканей.
Негативное воздействие стрептококков при постстрептококковом гломерулонефрите блокируется бактериостатиками (Кларитромицин, Тетрациклин, Клиндамицин, Хинупристин), которые не позволяют возбудителям синтезировать дочерние молекулы. Применение бактерицидных лекарственных средств не рекомендуется, так как они способствуют гибели стрептококков, выделению продуктов их распада и аллергической реакции.
Терапия, проводимая при остром постстрептококковом гломерулонефрите, проводится не без участия стероидов, которые подавляют иммунную систему. С этой целью назначают Гидрокортизон, Преднизолон, Адреналин, Дексаметазон. Подобным образом уменьшают количество иммунных комплексов.
Лечащий врач прописывает при постстрептококковом гломерулонефрите постельный режим и диету (стол №7). Последняя отличается от остальных столов небольшим количеством животных продуктов питания (мяса, молока, яиц) и соли. Откорректированный рацион предусматривает наличие разгрузочных дней. Низкокалорийная пища не нагружает ЖКТ, облегчает состояние почек и выделительной системы в целом.
Обязательно проведение профилактики в отношении лиц, находящихся рядом с больным, и выявление источника заражения. Врач назначает иммунодепрессивные препараты для предупреждения стрессов, вызванных длительной терапией и нефротическим синдромом. При возникновении осложнений лечение дополняется.
В начале терапии обязателен прием антибиотиков (Феноксиметилпенициллина), антигистаминных препаратов (Эритромицина). При остром постстрептококковом гломерулонефрите ограничивают потребление воды, и продуктов, содержащих животный белок. Противоотечная терапия осуществляется с помощью Гипотиазида, Нитропруссида Натрия, Гидралазина (инъекции), Диоксида и Фуросемида. Судорожный синдром при постстрептококковом гломерулонефрите блокируют посредством Диазепама.
Помимо перечисленных лекарственных средств назначают:
- Инсулин.
- Бикарбонат натрия.
- Глюкозу.
- Кальций.
- Метилпреднизолон.
- Гепарин.
- Ксанидил.
- Ангинал.
- Трентал.
- Лазикс.
- Строфантин.
- Эуфиллин.
- Реланиум.
- Сульфат магния.
- Хлоралгидрат.
- Диазепам.
В исключительных случаях нефролог назначает лечение кортикостероидами, но это рискованно при повышенном АД или скрытой форме развития постстрептококкового гломерулонефрита. Лечение подбирается каждому пациенту в индивидуальном порядке. Лечащий врач учитывает тяжесть заболевания, его форму, клиническую картину, сопутствующие патологии, особые нюансы (беременность, аллергию на медикаментозные препараты). Самолечение при постстрептококковом гломерулонефрите категорически запрещено. Неправильный подбор лекарственных средств способен усугубить ситуацию. При появлении первых гломерулонефритовых симптомов необходимо обратиться в клинику.
Прогнозы
Проникновение возбудителя в организм человека провоцирует повреждение гломерулы и микроскопических структур почки в целом. Устранение здоровых клеток организма аутоиммунными антителами при постстрептококковом гломерулонефрите обеспечивает цепную реакцию. Мозг думает, что выделительная система в опасности, производит новых «защитников», в результате чего количество иммунных комплексов увеличивается, а почечные канальцы еще больше повреждаются.
В большинстве случаев патология заканчивается выздоровлением и излечивается довольно быстро. Вызвать постстрептококковый гломерулонефрит способна неблагоприятная внешняя среда, к примеру, воздействие низких температур. Также нельзя забывать про отравление или инфекционные заболевания.
Отсутствие терапии ведет к возникновению негативных последствий. Функциональность почек у детей восстанавливается полностью. К сожалению, этого не происходит у взрослых. СФК у них часто остается сниженным.
Осложнения
Отсутствие своевременного лечения при постстрептококковом гломерулонефрите чревато:
- Острой почечной недостаточностью.
- Проблемами сердечно-сосудистой системы.
- Инфекционно-токсическим шоком.
- Инсультом.
- Гипертоническим кризом.
- Отеком легких.
- Почечной эклампсией.
- Сердечной астмой.
- Олигурией (анурией).
- Гиперкальциемией (гиперфосфатемией, гипонатриемией, гиперкалиемией).
- Ацидозом.
- Гипертензивной энцефалопатией.
Итогом постстрептококкового гломерулонефрита может стать инвалидность или даже летальный исход. При возникновении данных последствий лечащий врач назначает антигипертензивные медикаменты, среди них Нифедипин, Нитропруссид, Лабетолол, Гидралазин. Эклампсию лечат Дифенином и Фенобарбиталом. Против сердечной недостаточности и ее проявления, в частности, астмы подбирают соответствующую терапию. Гемодиализ является самой эффективной мерой при острой почечной недостаточности.
К симптомам, говорящим об усугублении ситуации, относят:
- Потерю сознания.
- Недержание урины.
- Высокое артериальное давление.
- Прерывистое дыхание.
- Цианоз кожных покровов.
- Отечность.
- Увеличение печени.
- Малокровие.
- Уремическую кому.
- Нарушения в ЦНС.
При их возникновении требуется дополнительная диагностика. Проблемы с сердцем чаще возникают у взрослых пациентов. Их игнорирование существенно уменьшает шансы на выздоровление при возникновении постстрептококкового гломерулонефрита.
Профилактика и прогноз
Здоровье человека в его собственных руках. Отсутствие своевременных мер даже при обычной «простуде» способно спровоцировать более серьезные патологии. Поэтому необходимо предупреждать развитие заболеваний дыхательных путей. Для этого следует избегать воздействия низких температур, не заниматься самолечением, укреплять организм.
Терапия при постстрептококковом гломерулонефрите в любом случае должна назначаться лечащим врачом. Он основывает принятые меры на результатах диагностических исследований. Предупредить патологии почек можно, соблюдая определенные правила:
- Регулярно проходите медицинское обследование.
- Правильно питайтесь (ограничьте потребление соли и животного белка).
- Не злоупотребляйте алкоголем и медикаментозными препаратами (если они подобраны самостоятельно).
- Избавьтесь от вредных зависимостей.
- Занимайтесь спортом.
- Закаляйтесь.
- Соблюдайте гигиену.
- Точно следуйте рекомендациям лечащего врача.
- Избегайте стрессовых ситуаций.
Живите полной жизнью, но при этом не переходите границ. Активный отдых, частые прогулки и хорошие эмоции вкупе с рекомендациями, перечисленными выше, помогут повысить качество жизни и укрепить иммунную систему.
После выздоровления пациент еще некоторое время находится на учете нефролога. Для взрослых людей срок составляет 24 месяца, для ребенка – 5 лет. Возврат постстрептококкового гломерулонефрита возможен, но при соблюдении здорового образа жизни маловероятен. Хорошим вариантом для реабилитации станет посещение санатория и профилактика заболеваний почек.
Используемые источники:
- https://pochkimed.ru/klubochkoviy-nefrit/ostryj-poststreptokokkovyj-glomerulonefrit.html
- https://pochkam.ru/bolezni-pochek/poststreptokokkovyj-glomerulonefrit.html
- https://alexmed.info/2017/01/09/острый-постстрептококковый-гломерул/
- https://mfarma.ru/mochepolovaya-sistema/bolezni-pochek/poststreptokokkovyj-glomerulonefrit